گلوکورونیداسیون
گلوکورونیداسیون (انگلیسی: Glucuronidation) فرایندی است که در جریان سوختوساز برخی مواد، از جمله داروها، آلودهکنندهها، بیلیروبین، آندروژنها، استروژنها، مینرالوکورتیکوئیدها، گلوکوکورتیکوئیدها، مشتقات اسید چرب، رتینوئید و نمکهای صفراوی صورت میپذیرد و پیوندهای گلیکوزیدی را نشانه میرود.[۱]
نحوهٔ عملکرد
[ویرایش]گلوکورونیداسیون شامل انتقال اسید گلوکورونیک از اوریدین دیفسفات گلوکورونیک اسید به یک سوبسترا توسط یکی از انواع آنزیمهای اوریدین دیفسفات-گلوکورونوزیلترانسفراز است.
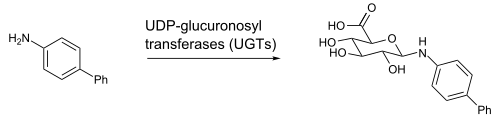
مادهٔ «اوریدین دیفسفات گلوکورونیک اسید» (که از طریق اتصال اسید گلوکورونیک توسط یک پیوند گلیکوزیدی به اوریدین دیفسفات حاصل میشود) یک مادهٔ واسط طی این واکنش شیمیایی است که در کبد حاصل میشود. یک مثال از این واکنش، اِن-گلوکورونیداسیون ۴-آمینوبیفنیل (نوعی آمین آروماتیک) توسط آنزیمهای UGT1A4 یا UGT1A9 در کبد انسان و موش است.
مادهای که طی فرایند گلوکورونیداسیون حاصل میشود، گلوکورونید است که حلالیت بسیار بیشتری از مواد فاقد اسید گلوکورونیک داراست. بدن انسان از این فرایند استفاده میکند تا برخی مواد و سموم را محلول در آب کرده و آن را از طریق ادرار و مدفوع دفع کند. دلیل گلوکورونیداسیون برخی هورمونها هم اسن است که انتقال آن به سرتاسر بدن تسهیل گردد. داروسازان، داروها را به اسید گلوکورونیک اتصال میدهند تا برخی انجام برخی درمانهای بالقوه، با تأثیرگذاری بیشتری انجام شود. برخی سموم نیز در اثر گلوکورونیداسیون، سمیت کمتری مییابند.
به فرایند اتصال موادِ بیگانهزیِ مضر به مولکولهای آبدوستی چون اسید گلوکورونیک، «فاز ۲ متابولیسم» گفته میشود.
مکانها
[ویرایش]گلوکورونیداسیون بیشتر در کبد صورت میپذیرد. با این حال، آنزیم مسئول فروکافت این واکنش، یعنی اوریدین دیفسفات-گلوکورونوزیلترانسفراز، در بافتهای دیگری همچون روده، کلیهها، مغز، غده فوق کلیوی، طحال و تیموس هم سافت شده است.
عوامل عمومی تأثیرگذار
[ویرایش]عوامل مختلفی در سرعت گلوکورونیداسیون و در نتیجه در کلیرانس مواد از بدن نقش دارند. معمولاً هرچه سرعت گلوکورونیداسیون بیشتر باشد، قدرت دارو یا مادهٔ مورد نظر در بدن کمتر میشود.
| عوامل | تأثیر بر گلوکورونیداسیون[۲] | ماده یا داروی مورد اثر[۲] | |
|---|---|---|---|
| سن | شیرخواران | ↑ | کلرامفنیکل، مرفین، استامینوفن، بیلیروبین، استروئیدها |
| افراد مسن | ↑ یا بدون تغییر | تغییری در استامینوفن دیده نشده است، اگزازپام، تمازپام، یا پروپرانولول. کاهش کلیرانس در کدئین-۶-گلوکورونید، و کاهش کلیرانس اُگزازپام در افراد بسیار پیر. | |
| جنسیت | مؤنث | ↓ | در جنس مذکر، کلیرانس برای داروهای استامینوفن، اگزازپام، تمازپام و پروپرانولول بیشتر است. به سبب اثر افزایشی احتمالی آنزیم CYP1A2، غلظت کلوزاپین و الانزاپین در جنش مؤنث بالاتر است. |
| مذکر | ↑ | ||
| هیکل و ساختار بدن | دارایِ اضافه وزن | ↑ | کلیرانس بیشتر استامینوفن، اگزازپام، تمازپام و لورازپام به دلیل احتمالی بزرگتر بودن کبد و افزایش محتوای آنزیمی آن |
| کموزنی/سوءتغذیه | ↓ | کلرامفنیکل، استامینوفن | |
| وضعیت سلامت/بیماری | هپاتیت برقآسا (فولمینانت)، سیروز | ↓ | زیدوودین، اگزازپام، لاموتریژین |
| کمکاری تیروئید | ↓ | اگزازپام، استامینوفن | |
| ابتلا به اچآیوی | ↓ | استامینوفن | |
| استعمال دخانیات | ↑ | پروپرانولول، اگزازپام، لورازپام، استامینوفن. به سبب اثر افزایشی احتمالی آنزیم CYP1A2، غلظت کلوزاپین و الانزاپین کاهش مییابد. | |
داروهای اثرپذیر
[ویرایش]بسیاری از داروهایی که سوبسترای گلوکورونیداسیون هستند، طی فرایند سوختوساز خود در بدن، توسط تحریککنندهها یا بازدارندههای آنزیمهای خاص خود، بهشدت تحت تأثیر این فرایند واقع شده و سطحشان بالا یا پائین میرود. برخی از این داروها به شرح زیر هستند:
| سوبسترا | بازدارندههای گلوکورونیداسیون[۲] | القاءکنندههای گلوکورونیداسیون[۲][۳] |
|---|---|---|
| مورفین |
|
|
| اگزازپام |
|
|
| بیلیروبین | ||
| استامینوفن |
|
|
| آندروسترون |
|
|
| کاربامازپین- ۱۰٬۱ ۱-ترانسدیول |
|
|
| کدئین |
|
|
| لاموتریژین |
| |
| لورازپام |
|
|
| تمازپام |
|
|
| تستوسترون | ||
| زیدوودین |
منابع
[ویرایش]- ↑ King C, Rios G, Green M, Tephly T (2000). "UDP-glucuronosyltransferases". Curr. Drug Metab. 1 (2): 143–61. doi:10.2174/1389200003339171. PMID 11465080.
- ↑ ۲٫۰ ۲٫۱ ۲٫۲ ۲٫۳ Unless else specified in boxes, then reference is: Liston, H.; Markowitz, J.; Devane, C. (2001). "Drug glucuronidation in clinical psychopharmacology". Journal of Clinical Psychopharmacology. 21 (5): 500–515. doi:10.1097/00004714-200110000-00008. PMID 11593076.
- ↑ Neil B. Sandson, Drug-Drug Interaction Primer
- مشارکتکنندگان ویکیپدیا. «Glucuronidation». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۴ فوریه ۲۰۲۱.