گلیکوزآمینوگلیکان
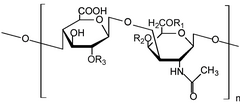

گلیکوزآمینوگلیکان (به انگلیسی: Glycosaminoglycan) یا موکوپلیساکارید پلی ساکاریدهای بدون شاخه طولانی میباشند که از تکرار واحدهای دیساکارید تولید میشوند و نقش کلیدی در ساختمان مولکولی و عملکرد غشا سیتوپلاسمی دارند. به غیر از کراتان سولفات، واحد تکراری آن از یک شکرآمینه در کنار اورونیک اسید یا گالاکتوز تشکیل شدهاست. گلیکوزآمینوگلیکانها به دلیل بسیار قطبی بودن و جذب آب، در بدن به عنوان روانساز یا ضربه گیر استفاده میشود.
موکوپلی ساکاریدوز گروهی از اختلال متابولیک است که در آنها تجمعهای غیرطبیعی گلیکوزآمینوگلیکانها به دلیل کمبود آنزیم رخ میدهد.
تولید
[ویرایش]گلیکوزآمینوگلیکانها از لحاظ جرم مولکولی، اجزای سازنده دی ساکارید و سولفات بسیار متفاوت هستند. دلیل این امر این است که سنتز گلیکوزآمینوگلیکانها مانند پروتئینها یا اسیدهای نوکلئیک طبق الگو هدایت نمیشود بلکه بهطور مداوم با پردازش آنزیمها تغییر میکند.
گلیکوزآمینوگلیکانها بر اساس ساختارهای دی ساکارید هسته به چهار گروه طبقهبندی میشوند. هپارین / هپاران سولفات و کندروایتین سولفات / درماتان سولفات در دستگاه گلژی ساخته میشوند، که در آن هستههای پروتئینی ساخته شده در شبکه آندوپلاسمی خشن پس از ترجمه به وسیله O-گلیکولیزاسیون توسط گلیکوزیل ترانسفرازهایی که پروتئوگلیکان را تولید میکنند، اصلاح میشود. کراتان سولفات پروتئینهای هسته را از طریق N-گلیکولیزاسیون یا O-گلیکوزیلاسیون پروتئوگلیکان اصلاح میکند. گروه چهارم گلیکوزآمینوگلیکانها، اسید هیالورونیک توسط آنزیم سنتزکننده غشای سراسری که بلافاصله زنجیره دی ساکارید را به صورت پویا ترشح میکنند ، سنتز میشود.
کندروایتین سولفات / درماتان سولفات با پروتئینهای اتصال دهنده هپارین، بهطور ویژه برهم کنش درماتان سولفات با فاکتور رشد فیبروبلاست FGF-2 و FGF-7 در تکثیر سلولی و ترمیم زخم دخیل هستند. کندروایتین سولفات / درماتان سولفات در ارائه پشتیبانی و چسبندگی در استخوان، پوست و غضروف اهمیت دارد. سایر عملکردهای بیولوژیکی کهکندروایتین سولفات / درماتان سولفات برای آنها شناخته شدهاست که وظایف مهم را بر عهده دارند، شامل مهار رشد آکسون و بازسازی در رشد CNS، نقش در رشد مغز، فعالیت نیتروژنیک و عفونت پاتوژن میباشد.
عملکرد
[ویرایش]کندروایتین سولفات/درماتان سولفات
هپارین طبیعی بدن درگرانولهای ترشحی ماست سلها قرارگیری و ذخیره میشود. هیستامین موجود در داخل گرانولها در pH داخل گرانول ها(۵٫۲–۶٫۰) پروتونه میشود (H2A2 +)، بنابراین اعتقاد بر این است که هپارین، که دارای باربسیار منفی است، وظیفه حفظ الکترواستاتیک و ذخیرهسازی هیستامین را دارد. در کلینیک، هپارین به عنوان ضد انعقاد خون تزریق و همچنین اولین راه حل برای بیماریهای ترومبوآمبولیک محسوب میشود. هپاران سولفات (HS) فعالیتها و کارکردهای بیولوژیکی متعددی، از جمله چسبندگی سلول، تنظیم رشد و تکثیر سلولی، فرایندهای رشد، اتصال سطحی لیپوپروتئین لیپاز و پروتئینهای دیگر به سلول، رگ زایی، تهاجم ویروسی و متاستاز توموردارد.
کندروایتین سولفات/درماتان سولفات با پروتئینهای اتصال دهنده هپارین، بهطور ویژه برهم کنشهای سولفات درماتان با فاکتور رشد فیبروبلاست FGF-2 و FGF-7 که در تکثیر سلولی و ترمیم زخم دخیل هستند، برهمکنش میدهد در حالیکه برهمکنشها با فاکتوررشد /فاکتور پخش مسیر سیگنالینگ را از طریق گیرنده آن فعال میکند. کندروایتین سولفات/درماتان سولفات در ارائه پشتیبانی و چسبندگی در استخوان، پوست و غضروف اهمیت دارد. سایر عملکردهای بیولوژیکی که کندروایتین سولفات/درماتان سولفات در آنها به ایفا کردن نقش کلیدی شناخته شده، شامل مهار رشد آکسون و بازسازی در توسعه CNS، نقش در رشد مغز، فعالیت نیتروژنیک و عفونت پاتوژن است.
کراتان سولفات
[ویرایش]یکی از کارکردهای اصلی دسته سوم گلیکوزآمینوگلیکانها، کراتان سولفات، حفظ هیدراتاسیون بافت است. کراتان سولفات در استخوان، غضروف و قرنیه چشم وجود دارد. در داخل قرنیه طبیعی، درماتان سولفات کاملاً هیدراته شدهاست در حالی که کراتان سولفات فقط تا حدی هیدراته است و نشان میدهد کراتان سولفات ممکن است به عنوان یک بافر کنترل شده پویا برای هیدراتاسیون رفتار کند. در حالتهای بیماری مانند دیستروفی قرنیه ای ماکولار، که در آن سطح گلیکوزآمینوگلیکان مانند کراتان سولفات تغییر میکند، از بین رفتن هیدراتاسیون درون استرومای قرنیه به نظر میرسد که علت کدری قرنیه باشد، بنابراین از فرضیه طولانی مدت مبنی بروابستگی شفافیت قرنیه به سطح مناسب سولفات کراتان حمایت میکند. گلیکوزآمینوگلیکان کراتان سولفات در بسیاری از بافتهای دیگر علاوه بر قرنیه نیز وجود دارد، که در آنها میتوانند چسبندگی ماکروفاژ را تنظیم کنند، موانعی برای رشد نوریت ایجاد کنند، لانه گزینی جنین در آستر رحم آندومتر در دورههای قاعدگی را تنظیم کنند و بر تحرک سلولهای اندوتلیال قرنیه تأثیربگذارند. بهطور خلاصه، کراتان سولفات نقش ضد چسبندگی ایفا میکند، که عملکردهای بسیار مهمی از کراتان سولفات را در تحرک و اتصال سلول و همچنین سایر فرایندهای بیولوژیکی بالقوه نشان میدهد.
درماتان سولفات
[ویرایش]درماتان سولفات در پوست، تاندونها، رگهای خونی و دریچههای قلب عملکرد دارد.
هیالورونیک اسید
[ویرایش]هیالورونیک اسید یکی از اجزای اصلی بافتهای سینوویال و مایعات و همچنین ماده زمینه سایر بافتهای همبند است. هیالورونیک اسید سلولها را به هم متصل میکند، مفاصل را روان میکند و به حفظ شکل مردمکها کمک میکند: ویسکوالاستیک بودن هیالورونیک اسید باعث میشود که برای روانکاری مفاصل و سطوحی که در امتداد یکدیگر حرکت میکنند مانند غضروف ایدهآل باشد. محلول هیالورونیک اسید تحت تنش برشی کم، ویسکوزیته بسیار بالاتری نسبت به زمانی که تحت تنش برشی بالا است، دارد. هیالورونیداز، آنزیمی که توسط سلولهای سفید خون، سلولهای اسپرم و برخی باکتریها ایجاد میشود، هیالورونیک اسید را از هم جدا میکند و باعث میشود محلول بیشتر مایع شود. در داخل بدن، هیالورونیک اسید کویلهای تصادفی به هم پیچیده را تشکیل میدهد که برای ایجاد یک شبکه هیالورونان به هم میپیچند، باعث کند شدن نفوذ و ایجاد یک سد نفوذی میشوند که حمل و نقل مواد بین سلولها را تنظیم میکند. به عنوان مثال، هیالورونان به تقسیم پروتئینهای پلاسما بین فضاهای عروقی و خارج عروقی کمک میکند، که در حلالیت ماکرومولکولها در داخل محوطه سلولی تأثیر میگذارد، تعادل شیمیایی را تغییر میدهد و ساختار الیاف کلاژن را تثبیت میکند.
ساختار
[ویرایش]گلیکوزآمینوگلیکانها پلی ساکاریدهای بدون شاخه طولانی میباشند که متشکل از واحدهای دی ساکاریدی هستند. این واحدهای دی ساکاریدی (بجز کراتین سولفات) عبارتند از یک هگزوزآمین (مانند ان استیل گلوکزآمین یا گالاکتوزآمین) و یک قند اورونیک مانند گلوکورونیک اسید یا گالاکتوز. فراوانترین آنها هیالورونیک اسید است. چهار گلیکوزآمینوگلیکان اصلی درماتان سولفات، کندروایتین سولفات، کراتان سولفات و هپاران سولفات هستند.
کارکرد
[ویرایش]گلیکوزآمینوگلیکانها در بافت همبند بیشتر حیوانات و گیاهان وجود دارند. این ترکیبات بسیار قطبی هستند و به دلیل جذب آب در بافتها دارای خاصیت لغزندگی و ضربه گیر هستند.
| Name | Hexuronic acid / Hexose | Hexosamine | Linkage geometry between predominant monomeric units | Unique features |
| کندروایتین سولفات | GlcUA or GlcUA(2S) | GalNAc or GalNAc(4S) or GalNAc(6S) or GalNAc(4S,6S) | 'GlcUAβ1-3'GalNAcβ1-4 | Most prevalent GAG |
| درماتان سولفات | GlcUA or IdoUA or IdoUA(2S) | GalNAc or GalNAc(4S) or GalNAc(6S) or GalNAc(4S,6S) | 'IdoUAβ1-3'GalNAcβ1-4 | Distinguished from chondroitin sulfate by the presence of ایدورونیک اسید، although some hexuronic acid monosaccharides may be اسید گلوکورونیک.[۱] |
| کراتین سولفات | Gal or Gal(6S) | GlcNAc or GlcNAc(6S) | -Gal(6S)β1-4GlcNAc(6S)β1-3 | Keratan sulfate type II may be fucosylated.[۲] |
| هپارین | GlcUA or IdoUA(2S) | GlcNAc or GlcNS or GlcNAc(6S) or GlcNS(6S) | -IdoUA(2S)α1-4GlcNS(6S)α1-4 | Highest negative charge density of any known biological molecule |
| هپاران سولفات | GlcUA or IdoUA or IdoUA(2S) | GlcNAc or GlcNS or GlcNAc(6S) or GlcNS(6S) | -GlcUAβ1-4GlcNAcα1-4 | Highly similar in structure to heparin, however heparan sulfate's disaccharide units are organised into distinct sulfated and non-sulfated domains.[۳] |
| اسید هیالورونیک | GlcUA | GlcNAc | -GlcUAβ1-3GlcNAcβ1-4 | The only GAG that is exclusively non-sulfated |
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- مشارکتکنندگان ویکیپدیا. «Glycosaminoglycan». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۲۱ فوریه ۲۰۱۴.
- ↑ Trowbridge JM, Gallo RL. (2002). "Dermatan sulfate: new functions from an old glycosaminoglycan". Glycobiology. 12 (9): 117R–125R. doi:10.1093/glycob/cwf066. PMID 12213784.
- ↑ Funderburgh JL. (2000). "Keratan sulfate: structure, biosynthesis, and function". Glycobiology. 10 (10): 951–958. doi:10.1093/glycob/10.10.951. PMID 11030741.
- ↑ Gallagher, J.T. , Lyon, M. (2000). "Molecular structure of Heparan Sulfate and interactions with growth factors and morphogens". In Iozzo, M, V. (ed.). Proteoglycans: structure, biology and molecular interactions. Marcel Dekker Inc. New York, New York. pp. 27–59. ISBN 978-0-8247-0334-9.
{{cite book}}: نگهداری یادکرد:نامهای متعدد:فهرست نویسندگان (link)
- Sasisekharan, Ram; Raman, Rahul; Prabhakar, Vikas (اوت ۲۰۰۶). "Glycomics Approach to Structure-Function Relationships of Glycosaminoglycans". Annual Review of Biomedical Engineering. 8 (1): 181–231. doi:10.1146/annurev.bioeng.8.061505.095745. PMID 16834555
- Funderburgh, JL. (2000). "Keratan sulfate: structure, biosynthesis, and function". Glycobiology. 10 (10): 951–8. doi:10.1093/glycob/10.10.951. PMID 11030741.Tortora, Gerard J. (2013-12-31). Principles of anatomy & physiology. Derrickson, Bryan (14th ed.). Danvers, MA. ISBN 978-1-118-34500-9.
- OCLC 871018672.Laurent TC, Laurent UB, Fraser JR (1996). "The structure and function of hyaluronan: An overview". Immunology and Cell Biology. 74 (2): A1-7. doi:10.1038/icb.1996.32. PMID 8724014.
- Sugahara K, Mikami T, Uyama T, Mizuguchi S, Nomura K, Kitagawa H (2003). "Recent advances in the structural biology of chondroitin sulfate and dermatan sulfate". Current Opinion in Structural Biology. 13 (5): 612–620. doi:10.1016/j.sbi.2003.09.011. PMID 14568617
- Rabenstein DL. (2002). "Heparin and heparan sulfate: structure and function". Natural Product Reports. 19 (3): 312–331. doi:10.1039/B100916H. PMID 12137280.
- Jin L, Abrahams JP, Skinner R, Petitou M, Pike RN, Carrell RW (1997). "The anticoagulant activation of antithrombin by heparin". Proceedings of the National Academy of Sciences of the United States of America. 94 (26): 14683-8 Bibcode:1997PNAS...9414683J. doi:10.1073/pnas.94.26.14683. PMC 25092. PMID 9405673.
- Rodén, L. (1989). Lane, DA (ed.). Heparin: Chemical and Biological Properties, Clinical Applications. CRC Press, Inc. p. 1.
