درگاه:شیمی/نوشتار برگزیده
نوشتار برگزیده ۱

گوگرد یکی از عناصر شیمیایی اصلی گروه ششم (VIA) در جدول تناوبی است. نماد آن S و عدد اتمی آن ۱۶ میباشد.اکتشاف این عنصر به پیش از تاریخ بازمیگردد.
گوگرد یک نافلز بیبو، بیمزه و چند ظرفیتی است که بیشتر به شکل کریستالهای زرد رنگ که در کانیهای سولفید و سولفات بهدست میآید شناخته شده میباشند. گوگرد یک عنصر حیاتی و لازم برای تمامی موجودات زنده میباشد و در ساختار اسید آمینوها و پروتئینها نیز هست. این عنصر به صورت اولیه در کودها استفاده میشود؛ ولی به صورت گستردهتر در باروت، ملیّنها، کبریتها و حشرهکشها نیز به کار گرفته میشود.
ادامه...
نوشتار برگزیده ۲

رنگرزی به فرایندی گفته میشود که در طی آن کالای نساجی مثل الیاف، نخ، پارچه یا پوشاک در محلولی که شامل مواد رنگزا و مواد شیمیایی میباشد، رنگ آمیزی گردد و مولکولهای رنگ، با دوامی نسبی با مولکولهای کالای نساجی، پیوند محکمی برقرار نمایند. به عبارت دیگر رنگرزی مهارتیاست که طی آن مادهٔ رنگزا در درجهٔ حرارت هدایت شده و زمان مشخص، داخل الیاف یا کالای منسوج (بافته شده) نفوذ کرده و آن را رنگ میکند. در رنگرزی، مادهٔ رنگزا به طور کلی، به همه مواد طبیعی یا شیمیایی که قابلیت رنگرزی الیاف یا منسوجات را دارند اطلاق میشود. رنگ کالای رنگرزی شده نباید به آسانی در اثر شستشو یا در برابر نور از بین برود. رنگرزی و چاپ دو روش رنگ کردن پارچه هستند که البته تفاوتهای اساسی با یکدیگر دارند. رنگرزی سنتی و رنگرزی صنعتی دو روش متداول رنگرزی میباشند. کاربری رنگرزی سنتی با نوین شدن صنعت نساجی، رفته رفته کاهش پیدا کردهاست. از نقاشیهای روی دیوارههای مقبرهها چنین استنتاج میشود که از بیش از ۳۰۰۰ سال قبل از میلاد مصریها حصیرهای رنگی میساختهاند. رنگرزی در ایران سابقهٔ کهنی دارد. کارگاه قالیبافی شاهان هخامنشی در شهر سارد و نوشتههایی دربارهٔ قالی ارغوانی رنگ، روی آرامگاه کوروش گواه این مدعا میباشد.
در فرایند رنگرزی چهار عامل نقش اصلی را بازی میکنند که عبارتند از: مواد رنگزا، کالای رنگرزی، مواد شیمیایی کمکی و ماشینهای رنگرزی. مواد رنگزایی که در رنگرزی استفاده میشوند ممکن است منبع طبیعی یا مصنوعی داشته باشند. رنگرزی یا چاپ کلاقهای، گرهای و کاتازوم سه سبک مختلف رنگرزی از لحاظ نحوهٔ ایجاد نقوش گوناگون برروی پارچه، میباشند.
ادامه...
نوشتار برگزیده ۳

فرانسیم با نام قدیمی اکا-سزیم یا اکتینیم K، عنصری شیمیایی با نماد Fr و عدد اتمی ۸۷ است که در گروه IA (فلزهای قلیایی) و دوره هفتم قرار گرفتهاست. این عنصر، یک الکترون ظرفیتی دارد و در میان همه عناصر جدول تناوبی، دارای کمترین الکترونگاتیوی است.دمای ذوب و جوش فرانسیم به ترتیب ۲۷ و ۶۷۷ درجه سانتیگراد، و شعاع اتمی آن ۲۷۰ پیکومتر است.
مارگوریت پری، فرانسیوم را در سال ۱۹۳۹ در فرانسه کشف کرد، به همین دلیل این عنصر فرانسیوم نام گرفت. این عنصر آخرین عنصر کشف شدهای است که در طبیعت به طور آزاد وجود دارد و پس از استاتین کمیابترین عنصر شناخته شدهاست.
فرانسیوم در بیرون از آزمایشگاه، به طور بسیار ناچیزی در سنگ معدن اورانیوم و توریوم یافت میشود، جایی که ایزوتوپ ۲۲۳ آن به طور پی در پی تشکیل و متلاشی میشود. تخمین زده میشود که حدود ۳۰ گرم فرانسیوم در پوسته زمین وجود داشته باشد. سایر ایزوتوپهای فرانسیوم به طور مصنوعی و در آزمایشگاه ساخته میشوند. بیشترین مقداری که تاکنون از فرانسیوم به طور مصنوعی ایجاد شده، یک خوشه ۱۰٬۰۰۰ اتمی بودهاست که از طریق ابر اتمی سرد و در دانشگاه استونی بروک و در سال ۱۹۹۷ ساخته شده است.فرانسیوم پس از فروپاشیدن به استاتین، رادیوم و رادون تبدیل میشود.
ادامه...
نوشتار برگزیده ۴

تاریخ شیمی به سلسله اتفاقاتی اطلاق میشود که از زمان باستان تاکنون برای دانش شیمی اتفاق افتادهاست. تا ۱۰۰۰ سال پیش از میلاد، تمدنهای باستان از ابزارهایی استفاده میکردند که سرانجام اساس تنوع شاخههای شیمی شدند. برای نمونه استخراج فلزها از سنگ معدن، سفالگری با استفاده از لعاب، تخمیر آبجو و شراب، تهیهٔ رنگدانه برای لوازم آرایشی و نقاشی، استخراج مواد شیمیایی از گیاهان برای دارو و عطر، تهیهٔ پنیر، ریسندگی، دباغی کردن چرم، تهیهٔ صابون از چربی، ساخت شیشه و ساخت آلیاژهایی مانند برنج.
در گذشته تلاش برای بیان طبیعت مواد و چگونگی دگرگونی آنها ناموفق بود. دانش پیشرفتهتر کیمیاگری نیز در این مورد ناتوان بود. به هرحال دانش کیمیا به کمک انجام تحقیقات اولیه و ثبت نتیجهها، پایهگذار شیمی مدرن بود. تغییر نگرش در شناخت مواد، زمانی شروع شد که رابرت بویل در سال ۱۶۶۱ در کتاب شیمیدان شکاک میان شیمی و کیمیا تفاوت قائل شد. پس از آن شیمی با تلاشهای آنتوان لاووازیه و ارائه قانون پایستگی جرم، به یک دانش تکاملیافته تبدیل شد. دغدغهٔ هر دو دانش کیمیا و شیمی شناخت طبیعت مواد و چگونگی دگرگونی آنها بود، اما تنها شیمی از شیوههای علمی قوی بهرهمند شد. با کوششهای ویژهٔ جوسایا ویلارد گیبز تاریخ شیمی با ترمودینامیک رابطهٔ عمیقی پیدا کرد.
تاریخ شیمی از آغاز تاکنون با صنعت رابطهای مستقیم داشتهاست. در ابتدای دوران مدرن در اروپا، شیمی از ترکیب دانستههای باستان با فعالیتهای دانشمندان مسلمان در قرون وسطی توسعه یافت. سپس شیمی در کنار فیزیک توانست ماهیت درونی مواد را شرح دهد.امروزه شیمی دانشی بسیار پیچیدهاست که بخشهای زیادی با اهداف متنوع در زمینههای مختلف فناوری دارد.
ادامه...
نوشتار برگزیده ۵

ابوبکر محمّد زَکَریای رازی (۲۵۱ ه.ق. – ۳۱۳ ه.ق.) پزشک، فیلسوف و شیمیدان ایرانی که آثار ماندگاری در زمینهٔ پزشکی و شیمی و فلسفه نوشته است و بهعنوان کاشف الکل و جوهر گوگرد (اسید سولفوریک) مشهور است.
به گفته جرج سارتن، پدر تاریخ علم، رازی «بزرگترین پزشک اسلام و قرون وسطی بود.» این دانشمند ایرانی از آنجا که کتابهای خود را به زبان عربی مینوشت، نزد غربیان به جالینوس عرب نیز مشهور بودهاست.
به پاس زحمات فراوان رازی در داروسازی روز پنجم شهریورماه (۲۷ اوت)، روز بزرگداشت زکریای رازی شیمیدان بزرگ ایرانی و روز داروسازی نامگذاری شده است.
ادامه...
نوشتار برگزیده ۶

چرخهٔ کربن چرخهای بیوژئوشیمی است که فرایند مداوم ترکیب و آزادسازی کربن و اکسیژن را در میان زیستکره، خاککره،آبکره، خاکسپهر و جو زمین توصیف میکند و در آن انرژی و حرارت ذخیره و دفع میگردد.همراه با چرخهٔ نیتروژن و چرخهٔ آب، چرخهٔ کربن نیز شامل دنبالهای از رویدادها است که باعث برقراری زندگی روی زمین میشود. چرخهٔ کربن نقش بسیار مهمی بر اثر گلخانهای و گرمشدن زمین دارد، از اینرو آگاهی یافتن از عملکرد آن، دخالت انسان در آب و هوا را ممکن ساخته و برای اندازهگیری تأثیر آن و یافتن پاسخی مناسب برای آیندهٔ زمین امری کلیدی بهشمار میرود.
کربن در طی چرخهاش به دو بخش سریع (کوتاهمدت) و کند (درازمدت) تقسیم میشود. چرخهٔ سریع کربن میتواند چند دقیقه تا چند سال را برگیرد؛ در مقابل آن چرخه کند کربن بازهٔ زمانی طولانیتری، چندین میلیون سال را دربر دارد. تفاوت اصلی بین چرخههای کند و سریع کربن در نوع ذخیرهسازی و مدتزمان آن است. چرخهٔ کربن برای اولین بار توسط جوزف پریستلی شیمیدان انگلیسی و آنتوان لاووازیه دانشمند فرانسوی کشف و توسط هامفری دیوی به عموم شناسانده شد.
از آغاز انقلاب صنعتی تاکنون، فعالیتهای انسان چرخهٔ کربن را به طور مستقیم با اضافهکردن کربن به جو زمین تغییر بسیاری دادهاست. استفاده از سوختهای سنگوارهای، جنگلزدایی، تغییر پوشش زمین، آلودگی هوا و خسارتهای گیاهی جزئی از این تغییرات هستند که تأثیر زیادی روی این چرخه گذاشتهاند. غلظت کربن دیاکسید در جو زمین از سال ۲۰۰۰ تا ۲۰۰۹ به طور سالانه ۲ پیپیام در حال افزایش بود و از تاریخ اکتبر ۲۰۱۲ به ۳۹۱ پیپیام رسیده است. با توجه به نمودارهای سنجش، این غلظت پیش از انقلاب صنعتی کمتر از ۲۸۰ پیپیام بود. سازمان جهانی دیدهبان جو در سال ۱۹۶۰ میلادی سازمان جهانی دیدهبان جو به منظور همین نگرانیها و کنترل جو زمین با هدف «مشاهدهٔ ترکیبات شیمیایی و خصوصیات فیزیکی جو زمین در مقیاسهای جهانی و منطقهای» تأسیس گردید که توسط سازمان جهانی هواشناسی و سازمان ملل متحد برنامهریزی و پشتیبانی میشود.
کربن دیاکسید در فتوسنتز مورد استفاده قرار میگیرد و نیز یک گاز گلخانهای برجسته است. با وجود غلظت نسبتاً کوچکش نسبت به دیگر گازها در اتمسفر بخش مهمی از جو زمین است که اشعه مادون قرمز را در طول موج ۴.۲۶ میکرومتر و ۱۴.۹۹ میکرومتر جذب و ساطع می کند، در نتیجه نقش مهمی در اثر گلخانهای دارد. سطح فعلی این گاز در اتمسفر بالاتر از هر سطح دیگری در طول تاریخ نسبت به ۸۰۰ هزارسال گذشته یا احتمالاً حتی ۲۰ میلیون سال گذشته رسیدهاست.
ادامه...
نوشتار برگزیده ۷

رادرفوردیم یک عنصر شیمیایی مصنوعی با نماد Rf و عدد اتمی ۱۰۴ است که به افتخار ارنست رادرفورد نامگذاری شدهاست. به عنوان یک عنصر مصنوعی، در طبیعت یافت نمیشود و تنها میتواند در یک آزمایشگاه ایجاد شود. این عنصر رادیواکتیو است و پایدارترین ایزوتوپ شناخته شده، ۲۶۷Rf، نیمه عمری حدود ۱ ساعت و ۱۸ دقیقه دارد. هر چند که گاهی نیمه عمر آن به ۵ ساعت هم میرسد.
در جدول تناوبی عناصر، یک عنصر در بلوک d و دومین عنصر واسطه و در گروه چهارم و در دوره هفتم است. آزمایشهای شیمیایی نشان میدهند که رادرفوردیم مانند هافنیم رفتار میکند. خواص شیمایی رادرفوردیم تنها تا حدودی مشخص شدهاند. آنها با خواص شیمیایی گروه ۴ همخوانی دارند، هرچند که برخی از محاسبات نشان دادهاست که مشخصات این عنصر به دلیل اثرات نسبیتی میتواند بهطور قابل توجهی متفاوت باشد.
در دهه ۱۹۶۰، مقدار کمی از رادرفوردیم درمؤسسه مشترک تحقیقات هستهای در اتحاد جماهیر شوروی سابق و آزمایشگاه ملی لارنس برکلی در کالیفرنیا تولید شد. اولویت کشف و به همین ترتیب نامگذاری این عنصر بین دانشمندان شوروی و آمریکایی مورد اختلاف قرار گرفت تا که در سال ۱۹۹۷، اتحادیهٔ بینالمللی شیمی محض و کاربردی (IUPAC) نام رسمی این عنصر را ایجاد کرد. نام این عنصر از نام ارنست رادرفورد برنده جایزه نوبل سال ۱۹۰۸ گرفته شد.
ادامه...
نوشتار برگزیده ۸

لایهٔ اُزون یا اُزونسپهر لایهای به ضخامت ۳۰۰ دابسون (۳ میلیمتر) در لایهٔ استراتوسفر هواکره است با غلظت بالایی از مولکول ازون (O۳)، که در سال ۱۹۱۳ توسط دو فیزیکدان فرانسوی به نامهای چارلز فابری و هنری بویسون کشف شد. این لایه با جذب ۹۹٫۹–۹۵ درصد پرتو فرابنفش خورشید، موجب ادامهٔ زندگی بر روی کرهٔ زمین میشود. لایه اُزون پرتوهای پرانرژی فرابنفش را جذب کرده و آنها را به شکل پرتوهای فروسرخ در میآورند و به سطح زمین میفرستند.
در اوایل سال ۱۹۳۰، ترکیباتی به نام کلروفلوئوروکربنها (سیافسیها) در ایالات متحده آمریکا اختراعشد و در صنعت و خانه مورد استفاده قرار گرفت. این ترکیبات به استراتوسفر راه یافتند و عناصر کلر و برم موجود در آنها طی واکنشهای شیمیایی موجب تخریب تدریجی لایهٔ اُزون شدند. به ویژه، لایهٔ اُزون بر فراز قطب جنوب به شدت کاهش یافتهاست.
چرخهٔ ازون-اکسیژن بیان میکند که پرتوهای فرابنفش به مولکول اکسیژن برخورد کرده و پیوند میان مولکولهای اکسیژن را میشکند. اتمهای حاصل با مولکول اکسیژن دیگری واکنش داده و مولکول ازون را تشکیل میدهند. سطح ازون با تغییر فصلها، وزش باد و تغییرات خورشید نیز تغییر مییابد. ۱۰ درصد مولکولهای ازون هواکره در لایهٔ تروپوسفر قراردارند و بر خلاف ازون موجود در استراتوسفر، آلاینده به شمار میآیند و آسیبهایی به بافتهای زیستی انسان و دیگر جانوران میرسانند.
ادامه...
نوشتار برگزیده ۹
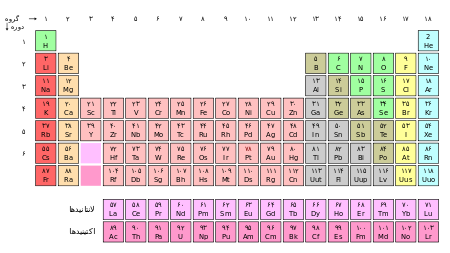
جدول تناوبی عنصرهای شیمیایی، نمایش جدولی عنصرهای شیمیایی بر پایهٔ عدد اتمی، آرایش الکترونی و ویژگیهای شیمیایی آنها است. ترتیب جایگیری عنصرها در این جدول از عدد اتمی (شمار پروتونهای) کمتر به سوی عدد اتمی بالاتر است. شکل استاندارد این جدول ۱۸ × ۷ است؛ عنصرهای اصلی در بالا و دو ردیف کوچکتر از عنصرها در پایین جای دارد. میتوان این جدول را به چهار مستطیل شکست، این چهار بلوک مستطیلی عبارتند از: بلوک اس در سمت چپ، بلوک پی در راست، بلوک دی (فلزات واسطه) در وسط و بلوک اف (فلزات واسطهٔ داخلی) در پایین. ردیفهای این جدول، دوره و ستونهای آن، گروههای جدول تناوبی نام دارند. همچنین گاهی برخی از این گروهها نامهای ویژهای دارند. برای نمونه گروه هالوژنها و گازهای نجیب از آن جملهاند. هدف از ساخت جدول تناوبی، چه به شکل مستطیلی و چه به شکلهای دیگر، بررسی بهتر ویژگیهای شیمیایی عنصرها بوده است. این جدول، کاربرد زیادی در دانش شیمی و پردازش رفتار عنصرها دارد.
جدول تناوبی با نام دیمیتری مندلیف شناخته شده است، با اینکه پیشروان دیگری پیش از او وجود داشتهاند. او این جدول را در سال ۱۸۶۹ منتشر کرد. این، نخستین جدولی بود که به این گستردگی مرتب شده بود. مندلیف این جدول را تهیه کرد تا ویژگیهای دورهای آنچه که بعدها «عنصر» نام گرفت را بهتر نشان دهد. وی توانسته بود برخی ویژگیهای عنصرهایی که هنوز کشف نشده بود را پیشبینی کند و جای آنها را خالی گذاشته بود. کمکم با پیشرفت دانش، عنصرهای تازهای شناسایی شد و جای خالی عنصرها در جدول پُر شد. با شناسایی عنصرهای نو و گسترش شبیهسازیهای نظری دربارهٔ رفتار شیمیایی مواد، جدول آن روز مندلیف بسیار گستردهتر شده است.
همهٔ عنصرهای شیمیایی از عدد اتمی ۱ (هیدروژن) تا ۱۱۸ (آناناکتیوم) شناسایی یا ساخته شدهاند. دانشمندان هنوز به دنبال ساخت عنصرهای پس از آناناکتیوم هستند و البته این پرسش را پیش رو دارند که عنصرهای تازهتر چگونه جدول را اصلاح خواهند کرد. همچنین ایزوتوپهای پرتوزای بسیاری هم در آزمایشگاه ساخته شده است.
نوشتار برگزیده ۱۰

پلاستیک به دستهای از مواد مصنوعی یا نیمه مصنوعی گویند که از فرایند بسپارش یا پلیمریزاسیون بدست میآیند. پلاستیکها دستهای از بسپارهای افزایشی یا تراکمی هستند. پلاستیکها را میتوان به شکلهای مختلف درآورد.
عمدتاً پلاستیکها برای عرضه به بازار به مواد کمکی متعددی از قبیل مواد ضد بلوک، آنتیاکسیدانها، عوامل ضدشکاف مانند پلیبوتادینها، پایدارکنندههای گرمایشی، لغزندهکنندهها، رنگها و تأخیراندازهای شعلهوری از قبیل آنتمران آغشته میکنند. پس از دفع پلاستیک به صورت زباله، هر یک از این مواد میتواند در اثر حرارت غذا با مواد غذایی وارد واکنش شیمیایی پلیمر شود.
ادامه...
نوشتار برگزیده ۱۱

اسید استیک با نام آیوپاک آن اتانوئیک اسید، جوهر انگور یا جوهر سرکه جز اسیدهای آلی (از گروه کربوکسیلیک اسیدها) است. فرمول آن CH3COOH است.
اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی، شبیه طعم سرکه میدهد.
این اسید یک اسید ضعیف بوده زیرا تنها مقداری اسید جدا شده در محلول آبی می باشد. استیک اسید بدون آب و خالص (استیک اسید یخی) یک مایع بدون رنگ بوده که آب را از محیط اطرافش جذب میکند(هیگروسکوپی) و در دمای 16.5 C(62 F) به شکل یک جامد کریستالی بی رنگ منجمد می شود. اسید خالص و محلول های غلیظ آن بسیار خورنده هستند.
استیک اسید یکی از ساده ترین کربکسیلیک اسید ها است. این اسید یک معرف شیمیایی مهم بوده و یک ماده شیمیایی صنعتی مورد استفاده در تولید مواد زیر است: پلی اتیلن ترفتالات که به صورت عمده در بطری های نوشابه استفاده می شود؛ سلولوز استات که به طور عمده در فیلم عکاسی استفاده می شود؛ پلی وینیل استات برای چسب چوب به علاوه فایبر ها و فابریک های مصنوعی. در خانه، استیک اسید رقیق برای بازکردن لوله ها استفاده می شود. در صنعت غذا، استیک اسید تحت کد افزودنی E260 به عنوان تنظیم اسیدی و به عنوان چاشنی استفاده می شود.
تقاضای جهانی استیک اسید در حدود 6.5 میلیون تن (متریک تن در سال Mt/a) که حدود 1.5 Mt/a از طریق بازیافت برآورده می شود. باقی آن توسط بازار خوراک پتروشیمیایی یا منابع بیولوژیکی تولید می شود. استیک اسید رقیق تولید شده توسط تخمیر طبیعی، سرکه نامیده می شود.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد.
ادامه...
نوشتار برگزیده ۱۲

مهارکننده آنزیم به مولکول هایی خطاب می شود که با اتصال به آنزیم ها، کاهش فعالیت آنها را در پی دارند. [۱] خیلی از داروها از این روش تاثیر میکنند مانند سولفونامید ، فیناستراید، نئوستیگمین و بازدارندههای آنزیم مبدل آنژیوتانسین. این مهار میتواند قابل برگشت یا غیرقابل برگشت باشد.
ادامه...
نوشتار برگزیده ۱۳

راکتور شیمیایی یا واکنشگاه شیمیایی وسیلهای است که در آن یک واکنش شیمیایی انجام میشود و طی آن مواد اولیه خام به محصولات تبدیل میشوند. طراحی و بهرهبرداری از راکتورهای شیمیایی از جمله مهمترین وظایف متخصصین صنایع شیمیایی از جمله مهندسین شیمی است. طراحی راکتور شیمیایی نیازمند شناخت درست از واکنش شیمیایی انجام گرفته در راکتور است و برای این منظور تسلط بر علومی چون ترمودینامیک شیمیایی، سینتیک شیمیایی و ریاضیات ضروری است. راکتورهای شیمیایی میتوانند در ابعاد بزرگ و برای مصارف صنعتی یا در ابعاد کوچک جهت کاربردهای آزمایشگاهی و تحقیقاتی ساخته و تولید شوند. همچنین جنبههای اقتصادی نیز بر طراحی بهینه راکتور تاثیر گذار است. از جمله صرف هزینه کمتر برای طراحی راکتور کاراتر و کوچکتر، صرف انرژی کمتر برای تولید محصول بیشتر، رساندن مواد اولیه به بیشترین درصد تبدیل و بالا بردن راندمان فرآیند و ... .در طراحی راکتورها پارامترهای زیادی از جمله:زمان اقامت()، حجم()، دما()، فشار()، غلظت گونههای شیمیایی()، ضریب انتقال حرارت (, )، سرعت واکنش ()و ... ، دخالت دارند. راکتورهای شیمیایی بر اساس نوع واکنش و موارد کاربرد در اشکال مختلف و با جزئیات خاص طراحی میشوند که پیچیدگی آنها را زیاد میکند. اما میتوان راکتورها را در چند دسته بزرگ و کلی از جمله راکتورهای پیوسته و ناپیوسته، راکتورها سیال بستر یا ثابت بستر، راکتورهای لولهای و مخزنی یا راکتورهای همگن و ناهمگن، طبقه بندی کرد. رفتار راکتورها معمولاً با معادلاتی موسوم به معادله راکتور مطرح میشود که برای گونههای مختلف راکتور متفاوت بوده و رابطه ریاضیاتی بین پارامترهای موثر در راکتور را بیان میکند.
ادامه...
نوشتار برگزیده ۱۴
نوشتار برگزیده ۱۵
نوشتار برگزیده ۱۶
نوشتار برگزیده ۱۷
نوشتار برگزیده ۱۸
نوشتار برگزیده ۱۹
نوشتار برگزیده ۲۰
نوشتار برگزیده ۲۱
نوشتار برگزیده ۲۲
نوشتار برگزیده ۲۳
نوشتار برگزیده ۲۴
نوشتار برگزیده ۲۵
نوشتار برگزیده ۲۶
نوشتار برگزیده ۲۷
نوشتار برگزیده ۲۸
نوشتار برگزیده ۲۹
نوشتار برگزیده ۳۰
نوشتار برگزیده ۳۱
نوشتار برگزیده ۳۲
نوشتار برگزیده ۳۳
نوشتار برگزیده ۳۴
نوشتار برگزیده ۳۵
نوشتار برگزیده ۳۶
نوشتار برگزیده ۳۷
نوشتار برگزیده ۳۸
نوشتار برگزیده ۳۹
نوشتار برگزیده ۴۰
نوشتار برگزیده ۴۱
نوشتار برگزیده ۴۲
نوشتار برگزیده ۴۳
نوشتار برگزیده ۴۴
نوشتار برگزیده ۴۵
نوشتار برگزیده ۴۶
نوشتار برگزیده ۴۷
نوشتار برگزیده ۴۸
نوشتار برگزیده ۴۹
نوشتار برگزیده ۵۰
نوشتار برگزیده ۵۱
نوشتار برگزیده ۵۲
نوشتار برگزیده ۵۳
نوشتار برگزیده ۵۴
نوشتار برگزیده ۵۵
نوشتار برگزیده ۵۶
نوشتار برگزیده ۵۷
نوشتار برگزیده ۵۸
نوشتار برگزیده ۵۹
نوشتار برگزیده ۶۰
نوشتار برگزیده ۶۱
نوشتار برگزیده ۶۲
نوشتار برگزیده ۶۳
نوشتار برگزیده ۶۴
نوشتار برگزیده ۶۵
نوشتار برگزیده ۶۶
نوشتار برگزیده ۶۷
نوشتار برگزیده ۶۸
نوشتار برگزیده ۶۹
نوشتار برگزیده ۷۰
نوشتار برگزیده ۷۱
نوشتار برگزیده ۷۲
نوشتار برگزیده ۷۳
نوشتار برگزیده ۷۴
نوشتار برگزیده ۷۵
نوشتار برگزیده ۷۶
نوشتار برگزیده ۷۷
نوشتار برگزیده ۷۸
نوشتار برگزیده ۷۹
نوشتار برگزیده ۸۰
نوشتار برگزیده ۸۱
نوشتار برگزیده ۸۲
نوشتار برگزیده ۸۳
نوشتار برگزیده ۸۴
نوشتار برگزیده ۸۵
نوشتار برگزیده ۸۶
نوشتار برگزیده ۸۷
نوشتار برگزیده ۸۸
نوشتار برگزیده ۸۹
نوشتار برگزیده ۹۰
نوشتار برگزیده ۹۱
نوشتار برگزیده ۹۲
نوشتار برگزیده ۹۳
نوشتار برگزیده ۹۴
نوشتار برگزیده ۹۵
نوشتار برگزیده ۹۶
نوشتار برگزیده ۹۷
نوشتار برگزیده ۹۸
نوشتار برگزیده ۹۹








