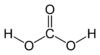
کربنیک اسید
| کربنیک اسید | |||
|---|---|---|---|
| |||
دیگر نامها محلول [ه[دیاکسید کربن]]، کربنات دی هیدروژن (IUPAC) | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۴۶۳–۷۹–۶ | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| خصوصیات | |||
| فرمول مولکولی | H2CO3 | ||
| جرم مولی | 62.03 g/mol | ||
| چگالی | 1.0 g/cm3 (محلول رقیق اما ضعیف) | ||
| انحلالپذیری در آب | exists only in solution | ||
| اسیدی (pKa) | 6.36 (see text) 10.25 | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| Infobox references | |||
|
| |||
کربنیک اسید (به انگلیسی: Carbonic acid) ترکیبی معدنی با فرمول H2CO3 و طبق طبقهبندی لوری و برونستد یک weak acidیا همان اسید ضعیف است که بهطور ناقص و ضعیف دچار یونش میشود.
کربنیک اسید را میتوان با افزودن مقداری HCL به ⁻CO3² بدست آورد در PH حدود ۳ علاوه بر آن در بدن از واکنش کربن دیاکسید و آب بدست میآید
همچنین کربنیک اسید از واکنش تعادلی دیاکسید کربن موجود در جَو با مولکولهای آب گازی شکل نیز به صورت آب پوشیده به دست میآید.
با فرمول:
CO2(g)+H2O(g)⇌H2CO3(aq)
افزایش میزان کربنیک اسید در خون باعث کاهش PH خون میشود. این تغییر PH باعث تغییر در ساختار پروتئینها میشود و میتواند عملکرد پروتئینها را مختل کند و به این دلیل که بسیاری از فعالیتهای یاخته را پروتئینها برعهده دارند باعث اختلال در فعالیتهای یاخته و بافتها میشود. در واقع افزایش کربن دیاکسید خطرناک تر از کاهش اکسیژن است.
منابع
[ویرایش]- مشارکتکنندگان ویکیپدیا. «Carbonic acid». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۲۰ فوریه ۲۰۱۴.