ویروپورین

ویروپورینها (به انگلیسی: Viroporin) پروتئینهای ویروسی چند منظوره، کوچک و معمولاً آبگریز هستند که نفوذ پذیری غشای سلولی را تغییر میدهند و در نتیجه آن، انتشار ویروس از سلولهای آلوده را تسهیل میکنند.[۲][۳] ویروپورینها میتوانند در کانالهای یونی الیگومری یا منافذ غشای سلولی میزبان جمع شوند و آن را نفوذپذیرتر و در نتیجه خروج ویریونها از سلول را تسهیل کنند. بسیاری از ویروپورینها همچنین اثرات اضافی بر متابولیسم سلولی و هموستاز دارند که با واسطه برهمکنش پروتئین-پروتئین با پروتئینهای سلول میزبان انجام میشود.[۳] ویروپورینها لزوماً برای تکثیر ویروس ضروری نیستند، اما سرعت رشد را افزایش میدهند. ژن این پروتئینها در انواع ژنومهای ویروسی وجود دارد اما در ویروسهای RNA بیشتر دیده میشود. بسیاری از ویروسهایی که باعث بیماری در انسان میشوند، توان بیان ژن ویروپورینها را دارند. این ویروسها شامل ویروس هپاتیت C، ویروس آنفولانزای A، ویروس فلج اطفال، HIV-1، ویروس سینسیشیال تنفسی و SARS-CoV هستند.[۳][۴][۵]
ساختار
[ویرایش]ویروپورینها معمولاً کوچک بوده (دارای کمتر از ۱۰۰ یا ۱۲۰ نوع آمینو اسید) و حاوی حداقل یک ناحیه با توانایی تا شدن به یک مارپیچ تراوای آمفی فاتیک هستند. برخی از نمونههای ویروپورین نیز بخشهایی دارای آمینو اسیدهای بازی یا آروماتیک بوده که تصور میشود در ناحیه سطحی غشاء قرار دارند.[۳] الیگومرهای این پروتئینها، اغلب تترامرها،[۶] کانالهای یونی یا منافذی با تراوایی یونی ضعیف تشکیل میدهند که اجازه انتشار یونها را در غشای سلولی میدهد. معماری مولکولی منافذ، میزان نفوذپذیری آن، میزان ترکیب لیپیدها در غشای اطراف و وجود بخشهایی از پروتئین که زوائد غشایی را تشکیل میدهند، همگی در بین ویروپورینها تفاوت دارد. این مسئله نشان میدهند که این پروتئینها دارای آرایه متنوع و نقشهای عملکردی مختلفی هستند.[۴][۵]
طبقهبندی
[ویرایش]یک طرح طبقهبندی پیشنهادی، ویروپورینها را بر اساس توپولوژی و جهتگیری آنها در غشاء سلولی به چهار دسته طبقهبندی میکند. ویروپورینهای «دسته I» تنها دارای یک مارپیچ نفوذپذیر و دو زیرگروه هستند. در زیرگروه «IA»، پایانه-C و در زیرگروه «IB» پایانه-N به سمت سیتوزول جهتگیری میکند. ویروپورینهای «دسته II» دارای یک موتیف مارپیچ-چرخشی-مارپیچ هستند که هر دو بخش مارپیچی از غشاء عبور میکنند. در زیرگروه «IIA» هر دو انتها به سمت خارج (برون سلولی یا به سمت لومِنِ شبکه آندوپلاسمی) و در زیرگروه «IIB» هر دو انتها به سمت سیتوزول قرار دارند.[۵] استثناهایی نیز برای این طبقه بندی ها وجود دارد مثلا پروتئین غیر ساختاری روتاویروس (VP4) در هیچیک از این دستهها چای نمیگیرد.[۷][۸]
عملکرد
[ویرایش]ضروری بودن
[ویرایش]اکثر ویروپورینها برای ویروسها ضروری نیستند، اما عدم وجود آنها بهطور قابل توجهی کارایی انتشار آنها را کاهش میدهد.[۹] پیامدهای مختلفی در کاهش تولید ویروپورین توسط ویروس وجود دارد برای مقال ویروس هپاتیت C بدون ویروپورین p7 قادر به تکثیر نیست، با این حال، توانایی تکثیر ویروس آنفولانزای A و HIV-1 در غیاب تِیتِر ویروسی خود در شرایط آزمایشگاهی همچنان وجود دارد اما ۱۰ تا ۱۰۰ برابر کاهش مییابد.[۴][۱۰] برخی از ویروسها در موارد نداشتن ویروپورین در ژنوم خود از توان حضور ویروپورین ویروسی دیگر در سلول استفاده و سرعت تکثیر خود را افزایش میدهند.[۵]
نفوذپذیری غشا
[ویرایش]تأثیر ویروپورینها در نفوذپذیری غشای سلولی به یونها و املاح کوچک به خوبی مطالعه و به اثبات رسیدهاست. قبل کشف تفاوتهای ساختاری و عماکردی در بین دستههای مختلف ویروپورینها، نقش آنها در افزایش نفوذ پذیری غشاء، در سلولهای آلوده، به خوبی شناخته شده بود. ویروپورین های ویژه در اواخر چرخه تکثیر ویروسی، مسئول اصلی تغییرات در غشا سلول هستند.[۲][۳][۱۱] ویروپورینهایی که به صورت تراریخته در آزمایشگاه تولید میشوند، در غیاب ویروس منشأ خود، میتوانند همچنان اثر خود را حفظ کنند و این ویژگی کشف ویروپورینها مختلف ویروسها را تسهیل کردهاست.[۵][۱۲]
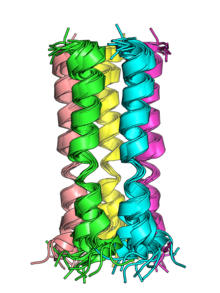
در بیشتر موارد، منافذ ایجاد شده توسط ویروپورینها غیرانتخابی هستند یا فقط برای یونهای خاص یا مولکولهای کوچک به مقدار کمی، تراوایی انتخابی دارند.[۱۰] اما برخی از ویروپورینهای قابلیت بسیاری در نفوذپذیری انتخابی از خود نشان میدهند. به عنوان مثال میتوان به پروتئین کانال پروتون M2 در ویروس آنفولانزا A که برای پروتونها بسیار انتخابی است و در pH پایین فعالیت میکند و پروتئین Kcv ودر یروس کلرلا که برای یونهای پتاسیم انتخابی است، اشاره کرد. همچنین یک مکانیسم جایگزینگر توسط پروتئین E موجود در SARS-CoV کشف شدهاست که در آن ویروپورین منافذی از لیپیدهای غشایی سلول میزبان را که سرهای قطبی آنها برای انتخاب یون ایجاد شدهاست، برای مصارف ویروسی تغییر میدهد.[۴] پروتئین E همولوگ SARS-CoV-2، که از نظر ساختاری با NMR حالت جامد مشخص میشود، یک پنتامر قابل نفوذ به کاتیونها را در غشاء سلول تشکیل میدهد.[۱۳][۱۴]
از دست دادن پلاریزاسیون غشاء میتواند بازده ویروس را از طریق مکانیسمهای مختلفی که در طول چرخه زندگی ویروسی عمل میکنند، افزایش دهد. در ویروسهای دارای پوشش، ویروپورینها به صورت تجمع یافته در پوشش ویروسی حضور ندارند، اما حضور آنها میتواند به ورود ویروس به سلول کمک کند. ویروس آنفولانزای A یک نمونه بررسی شده در ویروسهای پوشینهدار است. ویروپورینهای موجود در غشای اندامکهایی مانند دستگاه گلژی میتوانند محیط داخلی آن اندامکها را تحت تأثیر قرار دهند و قاچاق پروتئین از آن را برای ساخت اجزای ویروسی تعدیل کنند. همچنین میتوانند از ویروس در برابر pH پایین و اجزای ایمنی سلول محافظت کنند در ویروسهای بدون پوشش، تغییرات نفوذپذیری غشاء ممکن است برای القای لیز سلولی کافی باشد و این نفوذ پذیری به ویریونهای جدید اجازه خروج از سلول را میدهد. احتمال میرود در ویروسهای دارای پوشش، اثر دپلاریزاسیون ویروپورینها باعث افزایش تکثیر ویروس شود.[۴][۵] از بین رفتن کانالهای یونی یا عملکرد منافذ ویروپورینها، چه از طریق جهش، تغییر در نفوذ پذیری بدون ایجاد اختلال در سایر عملکردها یا داروهای مسدود کننده کانال، معمولاً انتشار ویروس را کاهش یا از بین میبرد.[۴]
همانندسازی ژنوم
[ویرایش]اکثر ویروسهایی که ویروپورینها را در ژن خود کد میکنند، میتوانند در غیاب ویروپورین همچنان ژنوم خود، حتی اگر در سرعت آن اختلال ایجاد شود، را همانندسازی کنند، با این حال، روتاویروسها و پیکورناویروسها برای تسهیل تشکیل ویروپلاسم یا بخشهای درون سلولیِ تخصصیِ بازسازیشده از غشای شبکه آندوپلاسمی که در آن تکثیر ژنوم اتفاق میافتد، به ویروپورینهای خود متکی هستند.[۵]
تعامل پروتئین-پروتئین
[ویرایش]برخی از ویروپورینها اثرات عملکردی را از طریق فعل و انفعالات پروتئین-پروتئین اعمال میکنند. به عنوان مثال در HIV-1 ویروپورین Vpu تکثیر ویروس را اگرچه مکانیسم مولکولی دقیق این برهمکنش مشخص نیست، از طریق برهمکنش با CD4 و تترین، تعدیل میکند.[۶][۷][۱۰] آگنوپروتئین در پلیوماویروس JC به عنوان یک ویروپورین علاوه بر نقشهای متعددش، از طریق تعامل با پروتئینهای ویروسی مانند پروتئین کپسید اصلی VP1 فعالیتهای تغییر غشائی را انجام میدهد.[۱۵]
نقش در بیماری
[ویرایش]عوامل بیماریزا
[ویرایش]ویروپورینها را نیز میتوان نوعی پاتوژن در نظر گرفت. در ویروسهایی که ویروپورینها ضروری نیستند، بیماریزایی و انتشارشان در غیاب ویروپورین، فراتر از سطح مورد انتظار کاهش مییابد. در برخی موارد، اثرات نفوذپذیری غشایی ویروپورینها، میتوانند مجموعهها پروتئینی مرتبط با فعالسازی ایمنی غیر اختصاصی را بیش از اندازه فعال کند که این اتفاق باعث بروز علائم بیماری از جمله التهاب میشود.[۴]
انکوپروتئینها
[ویرایش]پروتئین E5 پاپیلومای انسانی ۱۶ که کمترین مطالعه را در بین سه پروتئینهای انکوژن HPV دارد، در سال ۲۰۱۲ به عنوان یک ویروپورین شناخته شد.[۱۶] این اولین نمونه شناخته شده از یک ویروپورین انکوژنیک بود.[۷]
اهداف دارویی
[ویرایش]هر چند بسیاری از ترکیبات شیمیایی، دارای توانایی اثر گذاری بر انواع مختلف ویروپورینها، که با عملکرد کانالهای یونی سر و کار دارند، نیستند؛ بررسی برخی از ویروپورینها، که برای انتشار ویروس ضروری هستند، برای اهداف دارویی و توسعه داروهای ضد ویروسی بسیار پر طرفدار است.[۳][۱۰] با این وجود داروهای ساخته شده به این روش، کاربردهای بالینی نسبتاً اندکی دارند. آمانتادین، که در دهه ۱۹۶۰ کشف شد و برای مدتی در مورد آنفولانزای A مورد استفاده قرار میگرفت، نمونهای از داروی هدفگیرنده ویروپورین است.[۴][۱۷][۱۸] با این حال، بررسی کاکرین در سال ۲۰۱۴ فایده ای برای استفاده از آن در کودکان یا افراد مسن پیدا نکرد[۱۹] و CDC ایالات متحده داروهای این دسته را به دلیل جهشهای ایجاد شده در ویروس و به تبع مقاومت دارویی گسترده ویروس توصیه نمیکند.[۲۰]
مثالها
[ویرایش]ویروپورینها را میتوان در تعداد زیادی از ویروسها با طبقهبندیهای ژنومی و مکانیسمهای تکثیر مختلف یافت.
(ssRNA و ssDNA ژنوم تک رشتهای و dsRNA و dsDNA ژنوم های دو رشتهای هستند و مثبت یا منفی بودن آنها نشان دهنده سنس ویروس است.
این جدول ترکیبی از جدول ۱ تحقیقات گونزالس و همکاران. ۲۰۰۳،[۳] جدول ۱ از وانگ و همکاران. ۲۰۱۱،[۶] و جدول ۱، جعبه ۱، و جعبه ۲ از نیئوا و همکاران. ۲۰۱۲ را نشان میدهد[۵]
جستارهای وابسته
[ویرایش]- هولینها، پروتئینهای گذرنده منافذ کوچک تولید شده توسط باکتریوفاژهای dsDNA
- متالوپروتئیناز
- پروتئینهای حلقوی
منابع
[ویرایش]- ↑ Thomaston JL, Alfonso-Prieto M, Woldeyes RA, Fraser JS, Klein ML, Fiorin G, DeGrado WF (November 2015). "High-resolution structures of the M2 channel from influenza A virus reveal dynamic pathways for proton stabilization and transduction". Proceedings of the National Academy of Sciences of the United States of America. 112 (46): 14260–5. Bibcode:2015PNAS..11214260T. doi:10.1073/pnas.1518493112. PMC 4655559. PMID 26578770.
- ↑ ۲٫۰ ۲٫۱ Carrasco L (August 1995). "Modification of membrane permeability by animal viruses". Advances in Virus Research. 45: 61–112. doi:10.1016/S0065-3527(08)60058-5. ISBN 978-0-12-039845-4. PMC 7131156. PMID 7793329.
- ↑ ۳٫۰ ۳٫۱ ۳٫۲ ۳٫۳ ۳٫۴ ۳٫۵ ۳٫۶ ۳٫۷ Gonzalez ME, Carrasco L (September 2003). "Viroporins". FEBS Letters. 552 (1): 28–34. doi:10.1016/S0014-5793(03)00780-4. hdl:20.500.12105/7778. PMID 12972148. S2CID 209557930.
- ↑ ۴٫۰ ۴٫۱ ۴٫۲ ۴٫۳ ۴٫۴ ۴٫۵ ۴٫۶ ۴٫۷ Nieto-Torres JL, Verdiá-Báguena C, Castaño-Rodriguez C, Aguilella VM, Enjuanes L (July 2015). "Relevance of Viroporin Ion Channel Activity on Viral Replication and Pathogenesis". Viruses. 7 (7): 3552–73. doi:10.3390/v7072786. PMC 4517115. PMID 26151305.
- ↑ ۵٫۰ ۵٫۱ ۵٫۲ ۵٫۳ ۵٫۴ ۵٫۵ ۵٫۶ ۵٫۷ ۵٫۸ Nieva JL, Madan V, Carrasco L (July 2012). "Viroporins: structure and biological functions". Nature Reviews. Microbiology. 10 (8): 563–74. doi:10.1038/nrmicro2820. PMC 7097105. PMID 22751485.
- ↑ ۶٫۰ ۶٫۱ ۶٫۲ ۶٫۳ Wang K, Xie S, Sun B (February 2011). "Viral proteins function as ion channels". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1808 (2): 510–5. doi:10.1016/j.bbamem.2010.05.006. PMC 7094589. PMID 20478263.
- ↑ ۷٫۰ ۷٫۱ ۷٫۲ Luis Nieva J, Carrasco L (October 2015). "Viroporins: Structures and Functions beyond Cell Membrane Permeabilization". Viruses. 7 (10): 5169–71. doi:10.3390/v7102866. PMC 4632374. PMID 26702461.
- ↑ Hu L, Crawford SE, Hyser JM, Estes MK, Prasad BV (August 2012). "Rotavirus non-structural proteins: structure and function". Current Opinion in Virology. 2 (4): 380–8. doi:10.1016/j.coviro.2012.06.003. PMC 3422752. PMID 22789743.
- ↑ Gonzalez, Maria Eugenia; Carrasco, Luis (2005). "Viral proteins that enhance membrane permeability". In Fischer, Wolfgang B. (ed.). Viral membrane proteins : structure, function, and drug design. New York: Kluwer Academic/Plenum Publishers. pp. 79–90. doi:10.1007/0-387-28146-0_6. ISBN 978-0-387-28146-9. S2CID 81259776.
- ↑ ۱۰٫۰ ۱۰٫۱ ۱۰٫۲ ۱۰٫۳ González ME (August 2015). "Vpu Protein: The Viroporin Encoded by HIV-1". Viruses. 7 (8): 4352–68. doi:10.3390/v7082824. PMC 4576185. PMID 26247957.
- ↑ Carrasco L, Otero MJ, Castrillo JL (1989). "Modification of membrane permeability by animal viruses". Pharmacology & Therapeutics. 40 (2): 171–212. doi:10.1016/0163-7258(89)90096-x. PMID 2499894.
- ↑ Pinto LH, Holsinger LJ, Lamb RA (May 1992). "Influenza virus M2 protein has ion channel activity". Cell. 69 (3): 517–28. doi:10.1016/0092-8674(92)90452-I. PMID 1374685.
- ↑ ۱۳٫۰ ۱۳٫۱ Mandala, Venkata S. ; McKay, Matthew J. ; Shcherbakov, Alexander A. ; Dregni, Aurelio J. ; Kolocouris, Antonios; Hong, Mei (December 2020). "Structure and drug binding of the SARS-CoV-2 envelope protein transmembrane domain in lipid bilayers". Nature Structural & Molecular Biology. 27 (12): 1202–1208. doi:10.1038/s41594-020-00536-8. PMC 7718435. PMID 33177698.
- ↑ ۱۴٫۰ ۱۴٫۱ Cao, Yipeng; Yang, Rui; Lee, Imshik; Zhang, Wenwen; Sun, Jiana; Wang, Wei; Meng, Xiangfei (June 2021). "Characterization of the SARS‐CoV ‐2 E Protein: Sequence, Structure, Viroporin, and Inhibitors". Protein Science. 30 (6): 1114–1130. doi:10.1002/pro.4075. PMC 8138525. PMID 33813796.
- ↑ Suzuki T, Orba Y, Okada Y, Sunden Y, Kimura T, Tanaka S, Nagashima K, Hall WW, Sawa H (March 2010). "The human polyoma JC virus agnoprotein acts as a viroporin". PLOS Pathogens. 6 (3): e1000801. doi:10.1371/journal.ppat.1000801. PMC 2837404. PMID 20300659.
- ↑ Wetherill LF, Holmes KK, Verow M, Müller M, Howell G, Harris M, Fishwick C, Stonehouse N, Foster R, Blair GE, Griffin S, Macdonald A (May 2012). "High-risk human papillomavirus E5 oncoprotein displays channel-forming activity sensitive to small-molecule inhibitors". Journal of Virology. 86 (9): 5341–51. doi:10.1128/JVI.06243-11. PMC 3347351. PMID 22357280.
- ↑ Oxford JS (January 2007). "Antivirals for the treatment and prevention of epidemic and pandemic influenza". Influenza and Other Respiratory Viruses. 1 (1): 27–34. doi:10.1111/j.1750-2659.2006.00006.x. PMC 4634659. PMID 19453477.
- ↑ Oxford JS, Galbraith A (1980). "Antiviral activity of amantadine: a review of laboratory and clinical data". Pharmacology & Therapeutics. 11 (1): 181–262. doi:10.1016/0163-7258(80)90072-8. PMID 6159656.
- ↑ Alves Galvão MG, Rocha Crispino Santos MA, Alves da Cunha AJ (November 2014). "Amantadine and rimantadine for influenza A in children and the elderly". The Cochrane Database of Systematic Reviews. 2014 (11): CD002745. doi:10.1002/14651858.CD002745.pub4. PMC 7093890. PMID 25415374.
- ↑ "Influenza Antiviral Medications: Summary for Clinicians". Centers for Disease Control and Prevention. 6 May 2021. Retrieved 14 June 2021.
پیوند به بیرون
[ویرایش] پروندههای رسانهای مربوط به Viroporin در ویکیانبار
پروندههای رسانهای مربوط به Viroporin در ویکیانبار - پیوند به خانوادههای Viroporin در پایگاه داده TCDB
