سیتوز

سیتوز (انگلیسی: Cytosis) یک پسوند است که به جنبههای خاصی از سلول، مانند فرایند یا پدیده سلولی اشاره دارد و گاهی به غلبه نوع خاصی از سلولها دلالت دارد. این پسوند به معنای «مربوط به سلول» است. گاهی این واژه بهصورت کوتاه شده به شکل -وز (مانند نکروز (بافتمردگی)، آپوپتوز) یا مشابه برخی فرایندها که با -زیس تمام میشوند (مانند دیاپدزیس (تراگذری) یا امپریپولسیس، سیتوکینز) دیده میشود.
سه نوع اصلی سیتوز وجود دارد: اندوسیتوز (درونبَری، ورود به سلول)، اگزوسیتوز (برونرانی، خروج از سلول) و ترانسیتوز (ترارانی، عبور از سلول، ورود و خروج).
ریشهشناسی و تلفظ
[ویرایش]واژه cytosis (/saɪˈtoʊsɪs/) از ترکیب cyto- و -osis گرفته شده است و به سلول اشاره دارد. این اصطلاح اولین بار در سال ۱۹۶۱ توسط نوویکوف ابداع شد.[۱]
فرآیندهای مرتبط با ورود یا خروج زیرسلولی
[ویرایش]اندوسیتوز
[ویرایش]اندوسیتوز فرآیندی است که طی آن سلول یک مولکول، مانند پروتئین، را از خارج سلول جذب کرده و با غشای سلولی آن را احاطه میکند. این فرایند در اکثر سلولها استفاده میشود، زیرا بسیاری از مواد حیاتی به دلیل قطبیت شیمیایی بزرگ خود نمیتوانند از غشای سلول عبور کنند. دو نوع اصلی اندوسیتوز عبارتاند از پینوسیتوز و فاگوسیتوز.
پینوسیتوز
[ویرایش]پینوسیتوز (قطرهخواری)، یا نوشیدن سلولی، جذب ذرات آبی کوچک به همراه گیرندههای غشایی است که این ذرات را شناسایی میکنند. این فرایند نمونهای از اندوسیتوز فاز مایع است و معمولاً یک فرایند مداوم در سلول است. این ذرات از طریق حفرههای پوشیدهشده با کلاترین جذب میشوند. این حفرهها کوتاهمدت هستند و تنها برای تشکیل یک وزیکول برای انتقال ذرات به لیزوزوم خدمت میکنند. حفره پوشیدهشده با کلاترین به سیتوزول فرورفته و یک وزیکول پوشیدهشده با کلاترین را تشکیل میدهد. سپس پروتئینهای کلاترین از وزیکول جدا میشوند.[۲] آنچه باقی میماند بهعنوان اندوزوم اولیه شناخته میشود. اندوزوم اولیه با یک اندوزوم ثانویه ادغام میشود. این وزیکول اجازه میدهد ذرات جذبشده به لیزوزوم منتقل شوند، جایی که آنزیمهای هیدرولیتیک محتویات اندوزوم ثانویه را تخریب میکنند. گاهی بهجای تخریب، گیرندههایی که همراه با لیگاند اندوسیتوز شدهاند، به غشای پلاسما بازمیگردند تا فرایند اندوسیتوز ادامه یابد.
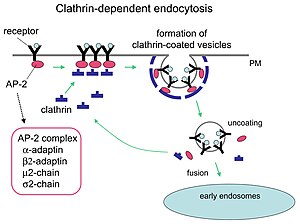
اندوسیتوز وابسته به گیرنده: این نوع از اندوسیتوز نوعی پینوسیتوز است. پروتئینهای پوشش کلاترین روی غشای پلاسما تمایل به اتصال و به دام انداختن ماکرومولکولها یا لیگاندها دارند. بااینحال، گیرندهها در حفره دلیل ایجاد پینوسیتوز نیستند. وزیکولها صرفنظر از حضور یا عدم حضور گیرندهها و لیگاندها تشکیل میشوند.[۳] به همین دلیل، پینوسیتوز یک رویداد مداوم و غیرتحریکی است، برخلاف فاگوسیتوز که در زیر توضیح داده میشود.
فاگوسیتوز
[ویرایش]فاگوسیتوز (بیگانهخواری)، یا خوردن سلولی، جذب ذرات بزرگتر مانند باکتریها به سیتوزول است. در موجودات تکسلولی کوچک، این فرایند روشی برای تغذیه است. در موجودات چندسلولی بزرگتر، این فرایند راهی برای تخریب سلولهای قدیمی یا آسیبدیده یا بلعیدن مهاجمان میکروبی است. در مورد بلعیدن باکتری، باکتری توسط پادتنها در محیط آبی به دام میافتد. هنگامیکه این پادتن به گیرنده روی سطح سلول برخورد میکند، غشای پلاسما با گسترش خود، باکتری را احاطه میکند؛ بنابراین، فاگوسیتوز یک رویداد تصادفی نیست. بلکه توسط اتصال یک لیگاند به گیرنده آغاز میشود.
برخی سلولها بهطور ویژه برای فاگوسیتوز طراحی شدهاند. این سلولها شامل سلولهای کشنده طبیعی، ماکروفاژها و نوتروفیلها هستند که همگی در پاسخ ایمنی نقش دارند و برای تخریب مواد خارجی یا آنتیژنی خدمت میکنند.[۴]
اگزوسیتوز
[ویرایش]
اگزوسیتوز (برونرانی) فرآیندی است که طی آن یک سلول محتوای ترشح وزیکول را به خارج از غشای سلولی هدایت میکند. وزیکولها با غشای سلولی ترکیب میشوند و محتوای خود را که معمولاً پروتئین است، به خارج از سلول آزاد میکنند.
دو نوع اگزوسیتوز وجود دارد: ترشح دائمی و ترشح تنظیمشده. در هر دو نوع، یک وزیکول از دستگاه گلژی جدا شده و به غشای پلاسمایی منتقل میشود تا از سلول آزاد شود. اگزوسیتوز لیزوزومها معمولاً برای ترمیم نواحی آسیبدیده غشای پلاسمایی با جایگزینی دولایه لیپیدی استفاده میشود.[۵]
ترشح دائمی (اگزوسیتوز غیرتنظیمشده)
[ویرایش]این حالت زمانی است که وزیکولی که از دستگاه گلژی جدا میشود، حاوی پروتئینهای محلول و همچنین لیپیدها و پروتئینهایی است که پس از ترکیب وزیکول با غشای پلاسمایی روی آن باقی میمانند. این نوع ترشح غیرتنظیمشده است. وزیکول در نهایت به غشای پلاسمایی منتقل شده و با آن ترکیب میشود. محتوای سلول به فضای خارجسلولی آزاد میشود، درحالیکه اجزای غشای وزیکول (لیپیدها و پروتئینهای غشای پلاسمایی) بهعنوان بخشی از غشای پلاسمایی سلول باقی میمانند.
ترشح تنظیمشده (اگزوسیتوز تنظیمشده)
[ویرایش]در این حالت، سلول سیگنالی از فضای خارجسلولی دریافت میکند، مانند یک ناقل عصبی یا هورمون، که ترکیب وزیکول با غشای پلاسمایی و آزادسازی محتوای آن را تنظیم میکند. وزیکول به غشای پلاسمایی منتقل میشود و تا زمانی که سیگنالی برای ترکیب با غشا و آزادسازی محتوا دریافت نکند، در آنجا باقی میماند.[۶]
ترانسیتوز
[ویرایش]ترانسیتوز نوعی از سیتوز است که به ذرات اجازه میدهد از یک غشا به غشای دیگر منتقل شوند. برای مثال، زمانی که یک گیرنده معمولاً روی غشای قاعدهای یا جانبی یک سلول پوششی قرار دارد، اما نیاز به انتقال به سمت غشای رأسی دارد، این کار فقط از طریق ترانسیتوز و به دلیل اتصالات محکم امکانپذیر است که مانع حرکت از یک ناحیه غشایی به ناحیه دیگر میشود. این نوع سیتوز معمولاً در اپیتلیوم، سلولهای رودهای و مویرگهای خونی رخ میدهد.
مولکولها یا موجودات بیماریزا نیز ممکن است از ترانسیتوز برای نفوذ به سلولها استفاده کنند. برخی مطالعات نشان دادهاند که باکتریها میتوانند از طریق ترانسیتوز سلولهای جامی به راحتی به داخل روده نفوذ کنند.[۷] از سوی دیگر، برخی تحقیقات در حال بررسی این ایده هستند که ترانسیتوز ممکن است به داروها اجازه عبور از سد خونی مغزی را بدهد و این ویژگی برای بهبود اثر درمانی برخی داروها استفاده شود.[۸]
پدیدههای مرتبط با تغییر یا حرکت سلولی
[ویرایش]- دیابدسیس: حرکت سلولهای خونی از لایه آندوتلیال.
- امپریپولسیس: ورود یک سلول به داخل سلول دیگر.
- تروگوسیتوز: اندوسیتوز دو غشا از یک سلول توسط سلول دیگر.
- افروسیس: فاگوسیتوز سلولهای آپوپتوتیک.
- سیتوکینز: آخرین مرحله تقسیم سلولی که طی آن دو سلول دختر از هم جدا میشوند.
پدیدههای مرتبط با غلبه سلولی
[ویرایش]- لکوسیتوز: افزایش تعداد لکوسیتها.
- ترومبوسیتوز: افزایش تعداد پلاکتها یا ترومبوسیتها.
- اریتروموسیتوز: افزایش تعداد گلبولهای قرمز که معمولاً بخشی از پلیسیتمی است و در آن توده کلی گلبولهای قرمز افزایش مییابد.
پدیدههای مرتبط با مورفولوژی سلولی
[ویرایش]- میکروسیتوز: قطر یا حجم کوچک سلولها، مانند گلبول قرمز در طبقهبندی کمخونی که به معنای غلبه میکروسیتها در تصویر خونی است.
- ماکروسیتوز: غلبه سلولهای بزرگتر (ماکروسیتها) در جمعیت سلولی (گلبولهای قرمز).
- آنایزوسیتوز: ناهمگنی در اندازه سلولها.
- اسفروسیتوز: غلبه سلولهای کرویشکل (اسفروسیتها) در جمعیت سلولی (گلبولهای قرمز).
- اووالوسیتوز: غلبه سلولهای بیضیشکل.
- دریپانوسیتوز: غلبه سلولهای داسیشکل در تصویر خونی.
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ Rieger, R. ; Michaelis, A. ; Green, M.M. 1991. Glossary of Genetics. Classical and Molecular (Fifth edition). Springer-Verlag, Berlin, [۱].
- ↑ Rappoport JZ (June 2008). "Focusing on clathrin-mediated endocytosis". The Biochemical Journal412 (3): 415–23. doi:10.1042/BJ20080474. PMID 18498251
- ↑ Mukherjee S, Ghosh RN, Maxfield FR (July 1997). "Endocytosis". Physiological Reviews 77 (3): 759–803. PMID 9234965
- ↑ Lodish, H. Berk, A. , Kaiser, C. , Kreiger, M. , Bretscher, A. , Ploegh, H. , Amon, A. , Scott, M. (2012) Molecular Cell Biology (7th ed.). W.H. Freeman and Co. New York: New York.
- ↑ Xu, J. , Toops, K. A. , Diaz, F. , Carvajal-Gonzalez, J. M. , Gravotta, D. , Mazzoni, F. , … & Lakkaraju, A. (2012). Mechanism of polarized lysosome exocytosis in epithelial cells. Journal of Cell Science 125(24): 5937-5943
- ↑ Lodish, H. Berk, A. , Kaiser, C. , Kreiger, M. , Bretscher, A. , Ploegh, H. , Amon, A. , Scott, M. (2012) Molecular Cell Biology (7th ed.). W.H. Freeman and Co. New York: New York.
- ↑ Nikitas, G. ; Deschamps, C. ; Disson, O. ; Niault, T. ; Cossart, P. ; Lecuit, M. (2011). "Transcytosis of Listeria monocytogenes across the intestinal barrier upon specific targeting of goblet cell accessible E-cadherin". Journal of Experimental Medicine 208 (11): 2263–2277. doi:10.1084/jem.20110560. متن کامل در PMC: 3201198. PMID 21967767
- ↑ Y. Joy Yu, et al. (2001). “Boosting Brain Uptake of a Therapeutic Antibody by Reducing Its Affinity for a Transcytosis Target”. Science Translational Medicine 3 (84): 84ra44. doi:10.1126/scitranslmed.3002230. PMID 21613623
- مشارکتکنندگان ویکیپدیا. «Cytosis». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۴ ژانویه ۲۰۲۵.
