سولفامیک اسید
| Sulfamic acid | |||
|---|---|---|---|
| |||
| |||
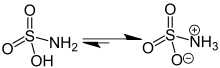
Sulfamic acid | |||
| شناساگرها | |||
| شماره ثبت سیایاس | 5329-14-6 | ||
| پابکم | 5987 | ||
| کماسپایدر | 5767 | ||
| شمارهٔ ئیسی | 226-218-8 | ||
| شمارهٔ یواِن | 2967 | ||
| ChEBI | CHEBI:9330 | ||
| ChEMBL | CHEMBL68253 | ||
| شمارهٔ آرتیئیسیاس | WO5950000 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| |||
| |||
| خصوصیات | |||
| فرمول مولکولی | H3NSO3 | ||
| جرم مولی | 97.10 g/mol | ||
| چگالی | 2.15 g/cm3 | ||
| دمای ذوب | 205 °C decomp. | ||
| انحلالپذیری در آب | moderate with slow hydrolysis | ||
| اسیدی (pKa) | 1.0[۱] | ||
| خطرات | |||
| MSDS | ICSC 0328 | ||
| شاخص ئییو | 016-026-00-0 | ||
| طبقهبندی ئییو | Irritant (Xi) | ||
| کدهای ایمنی | R36/38 R52/53 | ||
| شمارههای نگهداری | S۲ S26 S۲۸ S61 | ||
| ترکیبات مرتبط | |||
| دیگر کاتیونها | آمونیوم سولفامات | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| | |||
| Infobox references | |||
|
| |||
سولفامیک اسید (به انگلیسی: Sulfamic acid) با فرمول شیمیایی H۳NSO۳ یک ترکیب شیمیایی با شناسه پابکم ۵۹۸۷ است. که جرم مولی آن ۹۷٫۱۰ g/mol میباشد.
کاربردهای اسید سولفامیک
[ویرایش]اسید سولفامیک عمدتا ً یک ماده اولیه برای ترکیبات طعم شیرین است . واکنش با cyclohexylamine و به دنبال آن اضافه کردن naoh , C6H11NHSO3Na سدیم را ایجاد میکند . ترکیبات مرتبط همچنین شیرینکنندههای , مانند پتاسیم آسه سولفام هستند .
سولفامات ها در طراحی انواع مختلفی از عوامل درمانی مانند آنتیبیوتیکها , ویروس نقص ایمنی انسانی nucleoside / نوکلئوتید ( hiv ) مهار کنندههای ترانس کریپتاز معکوس , مهار کنندههای پروتئاز hiv ( PIs ) , داروهای ضد سرطان ( steroid و مهار کنندههای anhydrase ) , استفاده شدهاست .
عامل تمیز کننده
[ویرایش]عامل تمیز کردن سولفامیک اسید به عنوان یک عامل تمیز کننده اسیدی و عامل رسوب زدا گاهی خالص یا به عنوان جز مخلوطهای اختصاصی , به طور معمول برای فلزات و سرامیک استفاده میشود. برای اهداف تمیز کردن , عیارهای متفاوتی براساس کاربرد مانند عیار gp , عیار sr و tm وجود دارد . این روش اغلب برای حذف زنگ زنگ و آهک استفاده میشود و جایگزین اسید کلریدریک و آزار دهنده میشود که ارزانتر است . برای مثال , ژل ضخیم لیمو - a - way حاوی درصد اسید رسوب زدا است و دارای ph ۲.۰ - ۲.۲ , یا شوینده مورد استفاده برای حذف آهک است . در مقایسه با اغلب اسیدهای معدنی قوی , اسید سولفامیک دارای خواص مطلوب رسوب زدایی آب, نوسانات پایین و سمیت پایین است . این ماده نمکهای محلول در آب کلسیم , نیکل و آهن فریک را تشکیل میدهد.
این ماده دلیل ایمنی ذاتی خود در مصرف خانگی به هیدروکلریکاسید ترجیح داده میشود. اگر سهوا ً با محصولات مبتنی بر هیپوکلریت مانند سفید کننده مخلوط شود , گاز کلر تشکیل نمیدهد , در حالی که معمولترین اسیدها این است ; واکنش ( خنثی سازی) با آمونیاک , نمک تولید میکند.
همچنین در تمیز کردن صنعتی تجهیزات لبنی و آبجوسازی کاربرد دارد. اگرچه این ماده نسبت به اسید کلریدریک خورنده کمتری در نظر گرفته میشود , اما بازدارندههای خوردگی اغلب به تمیز کننده تجاری که جز آن است , اضافه میشوند . از آن می توان به عنوان یک رسوب زدا برای قهوه خانگی و ماشینهای اسپرسو و دندان های مصنوعی استفاده کرد.
سایر کاربردها
[ویرایش]- از کاتالیزور برای فرآیند استری کردن رنگ و رنگدانه تولید کننده علفکش رسوب زدا، برای حذف مقیاس مواد رزینهای اوره فرمالدهید در محیط اطفا حریق .
- اسید سولفامیک اصلیترین ماده خام برای آمونیوم سولفامات است که به طور گسترده از علفکش و مواد بازدارنده آتش برای محصولات خانگی استفاده میشود.
- صنایع خمیر و کاغذ به عنوان یک تثبیتکننده کلرید اکسید نیترو با واکنش با نیتریک اسید در آبکاری الکتریکی است .
- برای جداسازی یونهای نیتریت از مخلوط یونهای نیتریت و نیترات ( no3 - + no2 - ) در طول آنالیز کیفی نیترات با استفاده از آزمون حلقه قهوهای استفاده شد.
- به دست آوردن حلالهای یوتکتیک عمیق با اوره نقره با توجه به برچسب محصول مصرفکننده , محصول تمیز کننده نقره حاوی تیواوره , شوینده و اسید سولفامیک است.
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- ↑ Candlin, J. P.; Wilkins, R. G. (1960). "828. Sulphur–nitrogen compounds. Part I. The hydrolysis of sulphamate ion in perchloric acid". J. Chem. Soc. 0 (0): 4236–4241. doi:10.1039/JR9600004236. ISSN 0368-1769.
ویکیپدیا انگلیسی[۱]
- «IUPAC GOLD BOOK». دریافتشده در ۱۸ مارس ۲۰۱۲.
- ↑ "Sulfamic acid". Wikipedia (به انگلیسی). 2023-08-19.